前面说到铁的电化学反应,有朋友不理解, “说铁生锈应该是和氧气发生氧化反应导致的,物理课就是这样说的......”。其实他说的没错,但是这只是铁生锈的形式之一,且这种形式的生锈几乎可以忽略不计,事实上,铁生锈几乎都是电化学反应,请一定要记牢啊。
有朋友对电化学反应中的阴极和阳极也不太了解,所以还得再聊聊阴极和阳极。
> 阳极:在同一个电化学反应中,电位较低的金属或区域。
> 阴极:在同一个电化学反应中,电位较高的金属或区域。
>> 铁生锈时的阴极和阳极都是铁本身,出现了电位高低导致电化学反应。
>> 如果铁和铝材连接在一起,上面有冷凝水时,这时电化学反应的阴极和阳极就不都是铁,铝的电位更低,铁的电位更高,铝会生锈,而铁不会生锈。
以上两种情况,反应出:
>>> 在同一个电化学反应中,只要存在电位高低,就会出现阴极和阳极。
>>> 同一金属中,会出现电位高低;不同金属,电位也有高低,所以不管怎么组合,电位差肯定存在,条件一旦满足,就会引起电化学反应。
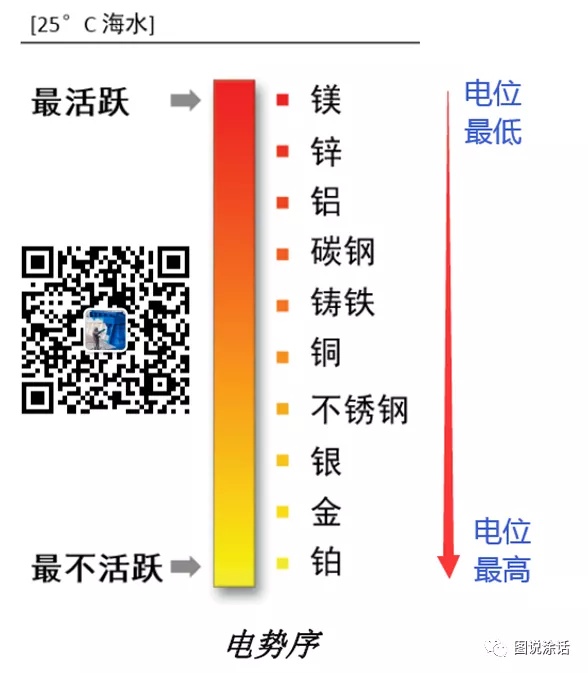
来看看不同金属的电位:
>>> 镁和锌连在一起,条件满足时,镁会生锈,锌不会生锈。
>>> 碳钢(铁)和铜连在一起,条件满足时,铁会生锈,铜不会生锈。
>>> 铜和银连在一起,条件满足时,铜会生锈,银不会生锈。
以上金属之间电位靠的比较近,电位差较小,电化学反应不会太激烈,但是 ......
>>> 镁和铂连在一起,条件满足时,镁会生锈,铂不会生锈,但是反应非常激烈、迅速。
这说明:电位差越大,反应越激烈;电位差越小,反应越和缓。
最后,再说下电化学反应中氧气的作用:
氧气基本上不与铁直接氧化反应,氧气在电化学反应中主要是去极化作用(消耗阳极流过来的电子),没有氧气的参与,电化学反应无法顺利进行。